Е.В. Москалёв
Кандидат технических
наук
Будь здоров, читатель,
или Как работают лекарства
От диагноза до таблетки
Что мы делаем, если чувствуем недомогание? Иногда идем к врачу, а чаще просто достаём домашнюю аптечку, берём таблетку, глотаем её и ждём результата Неприятные ощущения, как правило, проходят.
Но чтобы современное лекарство попало к нам в руки, тысячи людей работали, чтобы установить причины недугов, искали химические вещества, которые могут бороться с ними, действуя с минимальным ущербом для организма. Потом на лабораторных животных и сотнях добровольцев врачи отрабатывали оптимальную дозу лекарства. Лишь после долгих лет труда и бумажных волокит, которые занимают от пяти до десяти лет, новое лекарство разрешают к производству. А если учесть, что препарат ещё надо произвести, расфасовать, развезти по аптекам, рассказать о нём медицинским работникам Ну как тут не проникнуться уважением к создателям лекарств.
Достижения современной фармацевтики впечатляют. Пока в течение тысячелетий люди лечились отварами трав и прочими народными средствами, средняя продолжительность жизни человека была очень невелика. В средневековой Европе она не достигала и 40 лет, а сегодня, благодаря развитию здравоохранения и, в том числе новым лекарствам, почти удвоилась.
Эффекты и механизмы
С незапамятных времен люди знали: сок маковых головок снимает боль, напитки, приготовленные брожением зерна или фруктов, вызывают временные изменения в поведении, настойка коры ивы снижает повышенную температуру. Эти средства действовали всегда одинаково, независимо от причин, вызвавших боль или жар.
Но вот в середине XVII века обнаружили, что настойка коры хинного дерева
эффективно снимает жар у больных малярией, и попытались лечить этим
препаратом другие разновидности лихорадок. Однако выяснилось, что новое средство
оказывается в этом случае малоэффективным, да и на здоровых
людей оно тоже никак не влияет. Как же лекарство действует? Вопрос
этот долго оставался открытым, и только в 1880 г. французский
учёный Чарльз Лаверан установил, что малярию вызывает инфекционный
микроорганизм — малярийный плазмодий, который разрушает эритроциты,
а хинин подавляет его развитие
Сейчас мы знаем, что за регуляцию температуры тела отвечает
определённый участок мозга, который работает примерно как датчик
в термостате, — включая и выключая разогрев организма при потере
тепла. Паразиты попадают в кровь, продукты их жизнедеятельности
достигают мозга и устанавливают „датчик термостата“ на высокий уровень
разогрева. Лекарство же, со своей стороны, не дает плазмодию
размножаться, устраняя причину повышения температуры. Некоторое улучшение
самочувствия при других видах лихорадок наступает
Для большинства современных препаратов механизм действия хорошо
известен — и это важно. Ведь к одному и тому же
физиологическому эффекту
Рассмотрим это на примере. Мы знаем, как ведёт себя зрачок
по отношению к свету: при ярком освещении его диаметр уменьшается,
а в полутьме он становится больше. Некоторые лекарства, такие,
как атропин, если их закапать в глаза, действуют на мышцы,
управляющие адаптацией зрачка к световому потоку. Под действием атропина
зрачок расширяется, независимо от яркости света, а под влиянием
некоторых фосфоорганических продуктов
А вот если закапать в глаз раствор морфина, со зрачком ничего не случится, хотя хорошо известно, что при приёме наркотика внутрь происходит характерное сужение зрачка. Дело в том, что морфий влияет не на мышцы глаза, а на мозг и нервную систему, причём действует он подобно яркому свету. Из этого примера понятно, почему при создании новых лекарств учёные пытаются не только оценить очевидные эффекты от их приёма, но и понять, на какие органы и системы организма эти лекарства влияют, проследить метаболизм вещества. Только вся совокупность характеристик и позволяет чётко определить допустимую область применения препарата.
Если лекарство воздействует на орган как целое, объяснить механизм его работы обычно легко. Пример — нейтрализация избыточной кислоты желудочного сока с помощью соды, мела или гидроокисей алюминия и магния. Образующиеся продукты реакции, то есть соли, вода и углекислый газ, раздражают слизистую оболочку желудка значительно меньше, чем ионы водорода, и изжога прекращается. Другой пример — применение высокомолекулярного полимера гепарина для предотвращения свёртывания крови. Этот полимер содержит отрицательно заряженные сульфогруппы, которые легко реагируют с положительно заряженными белками плазмы крови. Комплекс гепарина с адсорбированными на нём белками не обладает свойствами исходных компонентов, и поэтому его коагуляция с последующим образованием тромбов просто невозможна.
Трудности с объяснением механизма действия лекарства могут возникнуть,
когда вещество регулирует работу не органов как таковых, а отдельных
клеток. Если
Лекарство и клетки
Чтобы разобраться с механизмом работы лекарств, действующих
на клеточном уровне, многие эксперименты с новыми препаратами ставят
даже не на животных, а на клеточных культурах.
Предшественники современных фармакологов установили, что существует определённая
связь между химической структурой лекарства и специфичностью его
биологического эффекта. Речь идёт в первую очередь о взаимодействии
лекарственного вещества с рецепторами на поверхности клеток. Такое
взаимодействие приводит к биологическому эффекту только при полном
соответствии функциональных групп в молекулах лекарства и рецептора,
то есть тогда, когда между ними образуются химические связи: ионные,
водородные или хотя бы обеспечиваемые силами
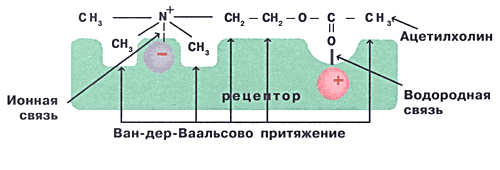
Рис.1 Схема взаимодействия молекулы
ацетилхолина со своим рецептором
Для специфичности и обратимости взаимодействия
Пытаясь разобраться, что представляют собой мембранные рецепторы и как
они работают, исследователи выделили из тканей рецептор ацетилхолина
в чистом виде. Оказалось, что это высокомолекулярный липопротеин.
В дальнейших исследованиях учёные подобрали химические вещества,
подходившие к рецептору как ключ к замку, способные связываться
с ним, и оказалось, что все они обладают в организме
той же фармакологической активностью, что и ацетилхолин
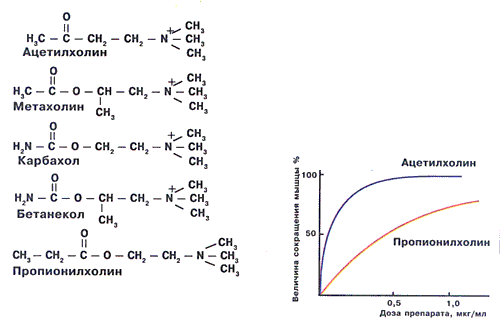
Рис.2 Молекулы, обладающие
в организме активностью ацетилхолина, имеют сходную с ним химическую
структуру. Неполное соответствие этих молекул структуре ацетилхолинового
рецептора клеточных мембран приводит к снижению эффективности
воздействия
Таким образом, выяснилось, что только вполне определённые химические группы
молекулы и их взаимное расположение действительно имеют значение
для того, чтобы вещество обладало биологическим эффектом. Другие звенья
молекулы можно было менять без особого ущерба для биоактивности. Это
открытие послужило толчком к синтезу лекарственных веществ, отличающихся
по своей структуре от природных регуляторов физиологических процессов.
Успехи химии хорошо видны на примере синтеза модифицированных эстрогенов
и аналогов прогестерона, которые совершили революцию в области
противозачаточных средств. Искусственно синтезированные аналоги имеют те же
активные центры, что и природные гормоны, у них та же
фармакологическая активность. Однако в отличие от природных, эти
вещества не разрушаются в кишечнике и печени с той же
лёгкостью: при оральном приеме они могут затем всасываться в кровь
и достигать
А сохранить биологическую активность вещества в организме
не
Например, один из основных белков плазмы крови — альбумин легко создаёт различные комбинации с антибиотиками, аспирином, сульфопрепаратами и многими другими лекарствами. По этой причине концентрацию таких веществ приходится увеличивать до тех пор, пока в крови не появится некоторое количество несвязанного препарата — только оно и пойдёт, собственно, на лечение.
В нашем обзоре мы не касаемся той группы химических веществ, механизм действия которых не связан со специфическими рецепторами напрямую, — это в основном анестетики. Строение молекул хлороформа, этилового спирта, закиси азота, циклопропана и инертного газа ксенона абсолютно различно, но все эти вещества воздействуют на мозг и вызывают порой схожие реакции.
Как преодолеть барьер
Обычно лекарства производят нужный эффект только тогда, когда достигают
непосредственно зоны действия — а именно рецепторов
на поверхности
Структуры, преграждающие путь молекулам лекарства, вообще говоря, полупроницаемы, то есть некоторые вещества проходят сквозь них свободно, другие с трудом, а для третьих они почти полностью непреодолимы. Это создаёт дополнительную проблему для фармакологии — ведь проходить через биологические барьеры способны только молекулы с подходящей конфигурацией.
Транспортный механизм в биологических системах подчиняется общим
законам, но имеет и свои особенности. Ведь для того, чтобы
лекарство подействовало, вещество должно не только более или менее свободно
проникать сквозь оболочки отдельных органов
Иногда лекарства просто диффундируют через мембраны, то есть
распространяются по градиенту концентрации. Однако есть и такие
вещества, которые могут накапливаться снаружи органа, но при этом почти
не проникают внутрь. Иногда они не могут достигнуть только
В подобных случаях разработчикам новых лекарств приходится учитывать и особенности конкретных органов, и структуру лекарственных агентов.
Как показали наблюдения, большинство лекарств являются электролитами. Причём
в отличие от сильных электролитов, к которым относятся
неорганические кислоты, щёлочи и соли, органические вещества ионизируются
в водном растворе только частично, образуя слабые кислоты, как аспирин:

или слабые основания, как норадреналин:

При этом степень ионизации, а значит, и растворимость лекарств
во многом зависит от рН среды. Это наблюдали, например, когда
исследовали свойства сильного яда стрихнина. В эксперименте лабораторным
животным вливали в желудок по 5 мг этого вещества в составе
растворов с разным уровнем рН. При рН 8,0 степень диссоциации молекул
стрихнина составляла 54% и животные погибали через 24 минуты, если раствор
имел рН 5,0
Выводы, которые следуют из результатов опыта, таковы: чтобы иметь
возможность пройти через липидную мембрану и попасть внутрь клетки,
некоторые вещества должны провзаимодействовать с заряженными группами
белков на поверхности мембраны
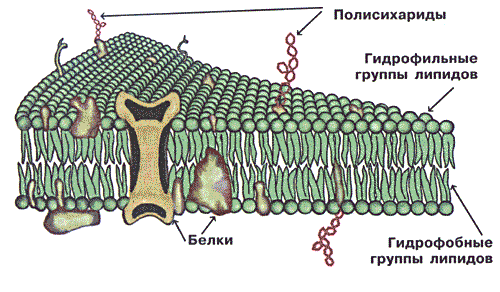
Рис.3 Структура клеточной мембраны
образовать с ними ионные или водородные связи
Функция некоторых белков в составе клеточных мембран заключается как раз
в том, чтобы переносить внутрь или наружу вещества, способные образовать
с ними связи. Однако основной способ доставки лекарств в клетку —
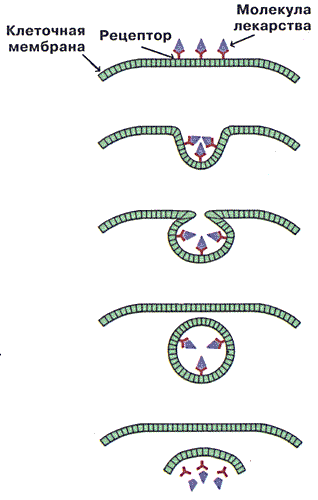 Рис.4 Последовательные
стадии эндоцитоза. В результате этого процесса молекулы лекарства
оказываются внутри клетки
Рис.4 Последовательные
стадии эндоцитоза. В результате этого процесса молекулы лекарства
оказываются внутри клетки
Однако каким бы ни был механизм проникновения лекарства через
мембрану в каждом конкретном случае, без первичного контакта с клеткой
молекулам никак не обойтись. Поэтому к двум первым задачам —
создать в молекуле центр, обеспечивающий лекарственный эффект препарата,
и не дать ей потерять активность раньше времени —
прибавляется третья: предусмотреть в структуре соединения функциональные
группы, способные обеспечить его активный перенос внутрь клетки. При этом
связывание с
По пути к месту действия
Итак, мы в общих чертах разобрались, как заставить молекулу лекарства работать на благо организма, а теперь самое время рассмотреть вопрос о том, как её доставить по назначению.
Наиболее удобный способ приема лекарства — это конечно же проглотить его, но этот вариант годится не всегда. Ведь в этом случае неизбежны колебания концентрации лекарства в организме: резкое увеличение после приёма и падение почти до нуля перед приёмом следующей дозы, причём состав пищи или её отсутствие в желудке иногда могут ещё больше обострить ситуацию.
Кроме того, среда в желудке очень агрессивная. Мало того что желудочный
сок имеет высокую кислотность
Исключение составляют вещества, которые вызывают раздражение внутренней
оболочки органов пищеварения, — их принимают после еды, чтобы защитить
желудок. В этом случае препарат усваивается, конечно, не сразу,
большая его часть попадает в кишечник вместе с пищей.
Но лекарственное вещество может всасываться и здесь, причём
в
Кстати, благодаря способности многих веществ эффективно проникать
в кровь через стенки прямой кишки можно вообще избежать воздействия кислой
среды желудка на препарат. В медицине давно и вполне успешно
применяют ректальные
Подкожное или внутримышечное введение лекарства решает те же проблемы:
избавляет лекарство от контакта с желудочным соком и позволяет
пощадить пищеварительный тракт. С помощью инъекций в мышцы ягодиц или
верхней части руки можно вводить большие объемы растворов,
да и барьерами для лекарств в этом случае будут только
стенки капилляров. Ну а на крайний случай есть и совсем
прямой путь: можно ввести препарат в кровоток, сделав больному внутривенную
инъекцию. При этом желаемый эффект получается куда быстрее. Ведь скорость,
с которой лекарства достигают
Однако даже если лекарство тем или иным образом попало в кровь, это ещё не означает, что все сложности с его транспортировкой к органам уже позади. Кровеносная система устроена так, что поток крови направляется от желудка и кишечника прямиком к печени и только потом поворачивает к другим органам. Это всегда учитывают при разработке новых лекарственных форм: ведь одна из функций печени — обезвреживать потенциально опасные соединения, значит, здесь могут разрушаться и лекарства.
Чтобы обойти печень, некоторые препараты рекомендуют класть под язык или рассасывать. Дело в том, что поток крови, обслуживающий полость рта, в своём первом цикле не проходит через печень, и активность вещества, проникающего в кровоток сквозь тонкий слой эпителия, сохраняется. Яркий пример — действие нитроглицерина. Таблетка, помещённая под язык, снимает сердечную боль в течение двух минут, а такое же количество препарата, принятое внутрь, для сердечника абсолютно бесполезно.
Иногда, чтобы не дать препарату быстро разрушиться, его вводят
в состав мази, которую втирают в кожу подходящего участка тела. Пройдя
сквозь несколько слоёв эпителия, лекарство сразу же попадает
в кровоток, направленный к больному органу. Трансдермальный путь
доставки лекарств хорош ещё и тем, что, используя вместо мази лечебный
пластырь, можно добиться поступления препарата в нужное место
с постоянной скоростью и очень точно соблюсти рекомендуемую дозу
Но если лекарственное вещество можно перевести в газообразное состояние
или оно представляет собой летучую жидкость, то лучший способ введения
препарата конечно же ингаляция. Тончайшая
Куда девать ненужное
Итак, мы уяснили себе, какими особенностями должны обладать вещества, претендующие на роль лекарств, поняли, как их доставить в нужную точку организма и заставить работать. Однако остаётся ещё один комплекс проблем. Как долго работает лекарство? Что происходит с ним потом? Как вывести чужеродное вещество из организма?
В большинстве случаев, как уже упоминалось, лекарственные вещества разрушаются в печени — организм стремится очиститься от чужеродных химикатов сам. При этом сложные соединения превращаются, как правило, в более простые вещества, способные выводиться из организма достаточно легко.
Например, некоторые альдегиды и спирты частично выходят через легкие. Этим пользуются сотрудники автоинспекции: если заставить нетрезвого человека подышать в трубочку с раствором вещества, реагирующего с продуктами распада алкоголя, можно определить степень опьянения водителя.
Небольшая доля водорастворимых лекарств и продуктов их метаболизма
удаляется из организма с потом, слезами, слюной и даже
с материнским молоком. Однако больше всего чужеродных веществ
и продуктов их распада концентрируется в моче. За день через
почки проходит около 180 литров жидкости, содержащей растворённые
вещества — большей частью, необходимые организму. При этом только
незначительная часть соединений
Разрушение лекарств этим органом — головная боль разработчиков новых препаратов. Но если вещество уже сыграло свою роль, то в дальнейшем печень очищает организм от продуктов метаболизма, что хорошо.
Каждый день печень нарабатывает до литра желчи, компоненты которой,
особенно желчные кислоты, способствуют разложению и усвоению жиров
в кишечнике. При этом более 80% печёночного секрета довольно быстро
всасывается в кровь и попадает из кишечника обратно
в печень. Таким образом, желчные кислоты совершают циркуляцию и могут
использоваться организмом повторно. Вот
Печень имеет в своём составе специальные клетки, внутри которых много так называемых микросомальных ферментов. В отличие от прочих, как правило, высокоспецифичных ферментов представители этой группы могут взаимодействовать с веществами очень разными по структуре. Обычно они переводят лекарственное вещество в неактивную форму, окисляя или восстанавливая молекулы.
Биотрансформация лекарственных веществ происходит не только в печени, но и в плазме крови, почках, тканях мозга, поскольку и внутри клеток, и на их поверхности, и во всех биологических жидкостях организма присутствует множество ферментов. А ферменты — это катализаторы химических реакций, в том числе и тех, в которых могут участвовать молекулы лекарств.
Итак, мы вкратце проследили путь лекарственной молекулы в организме от начала до конца. Надеюсь, читатели увидели, что между химической структурой лекарства и специфичностью его биологического действия существует определённая зависимость. Современные препараты обладают высокой избирательностью: они влияют только на определённые ткани, органы и даже клетки, в то время как на других частях организма их влияние может не сказываться вовсе.
Вот эту избирательность действия фармацевтическая наука и старается усовершенствовать. В последние годы для создания новых лекарств химики часто используют достижения молекулярной биологии. Поведение клеток под влиянием различных веществ задаёт направление поисков по созданию новых соединений — тех, которые будут действовать с минимальными побочными эффектами. Но такие разработки дороги, и, скорее всего, в перспективе новых лекарств будут создавать меньше, чем раньше. Весьма вероятно, что в ближайшем будущем фармакологическая химия сосредоточит внимание на совершенствовании методов синтеза уже известных лекарств.
„Химия и жизнь — XXI век“
